产品搜索
技术文章 / article
美国FDA《无菌工艺药品cGMP工业指南(2004年)》对洁净室污染控制的要求
2019-12-16 浏览次数:932
在无菌生产加工厂房中,应适当控制分隔的或划定的生产操作区,以达到生产操作所要求的不同空气质量级别,指定生产区的设计包括生产区要符合暴露设备、组分及产品所规定的微生物及微粒标准,以及进行操作活动时的微生物及微粒标准。
洁净区的控制参数应由确认试验中所得到的微生物和微粒数据来证实。洁净区的初步确认中包括完工时静态条件下空气质量评估的部分内容。生产区的确认以及级别划分最重视的是在动态条件下所得到的数据。适当的无菌生产厂房的监测方案也要评估其在动态条件下能够符合规定的洁净区级别。
下表总结了洁净区的空气级别划分以及需要采取措施的微生物水平。
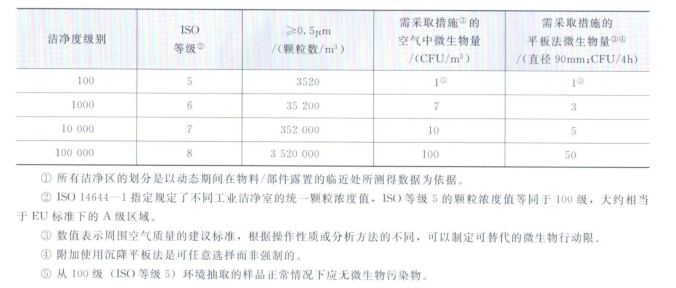
对无菌药品质量特别重要的有两个洁净区:关键生产区及与之相关联的辅助洁净区。
1、关键生产区--100级
关键生产区是无菌药品、容器及密封件露置的生产区,环境状况的设计必须保持产品的无菌性。在这些生产区所进行的操作包括在灌装及封口操作前及期间的无菌物料的处理。这类生产区之所以重要是因为露置的产品易于受污染,而且随后在其直接接触的容器内不再进行灭菌。为保持产品无菌,就必须对进行无菌操作的环境加以控制并保持适当的质量要求。环境质量的一项内容是空气中的微粒数。微粒是最重要的,因为它们可以进入产品,形成外来污染物,而且也会作为微生物载体污染产品。设计合适的空气处理系统可最大限度的降低关键生产区的微粒数。
建议对关键生产区空气洁净级别的测定要在对暴露的无菌产品、容器和密封件最为有潜在危险的地方进行。颗粒计数探头应放置在经证明可得到有价值的地方。每一班应进行日常的监测。建议用遥控计数系统监测非生物微粒。
2、辅助洁净区
辅助洁净区可以有不同的洁净级别及功能。许多辅助生产区的功能是用作准备、贮存或运送非无菌组分、配制产品、生产过程中间物料、设备及容器/密封件的区域。这些区域的环境可最大限度的减少成品中的微粒污染量,而且控制了随之灭菌的部件及组分的微生物量。
在辅助洁净区进行的工作性质决定了其级别的划分。FDA建设直接邻近无菌生产加工线的区域,在动态条件情况下至少要达到10000级标准。生产单位也可以把这一生产区域划分为1000级或保持整个无菌灌装室在100级。对一些非关键生产工作区可划分为100000级的空气洁净级别区域。


